北京百奥思科生物医学技术有限公司品牌商
8 年
手机商铺
- NaN
- 0.7000000000000002
- 0.7000000000000002
- 1.7000000000000002
- 0.7000000000000002
公司新闻/正文
多组学技术:解码脑肠轴信号,开辟心理压力性肠健康干预新路径
813 人阅读发布时间:2025-05-21 14:51
心理压力已成为现代社会的普遍问题,影响着约 30% 的成年人,并引发一系列健康问题,尤其是胃肠道疾病,如肠易激综合征(IBS)和炎症性肠病(IBD)。这些疾病不仅严重影响生活质量,还带来巨大社会经济负担。
近期研究发现,心理压力可通过触发单核细胞介导的肠道炎症加剧 IBD,初步揭示了精神压力对肠道炎症的作用机制。但肠道如何感知来自大脑的远端压力信号,以及哪些关键分子将调控指令传递给肠道上皮并导致功能紊乱,仍亟待解答。
2024 年,中国药科大学郝海平团队与东南大学附属中大医院袁勇贵团队合作,在《Cell Metabolism》(IF32.2)发表研究。通过宏基因组学、代谢组学、谱系追踪和代谢生物工程技术,研究证实:鼠乳杆菌衍生的吲哚-3-乙酸酯(IAA)是介导压力信号的关键分子,可触发肠道干细胞(ISC)向分泌谱系分化的内在缺陷。而补充α-酮戊二酸(α-KG)能有效缓解压力诱导的肠道上皮损伤。该研究揭示了微生物介导的 ISC 命运调控新途径,为解析压力驱动的脑肠轴疾病提供了重要机制依据。

研究内容
1、慢性压力干扰肠道干细胞分化与线粒体稳态
为探究心理压力对肠道健康的影响,团队构建慢性束缚应激(CRS)小鼠模型,结合Lgr5谱系追踪及单细胞测序等技术发现,CRS可导致小鼠肠道绒毛和隐窝减少、杯状细胞数量下降。Lgr5谱系追踪显示压力抑制肠道干细胞(ISCs)后代生成能力。RNA-seq和单细胞测序表明,CRS会降低线粒体氧化磷酸化能力、减少线粒体嵴并打破稳态,同时削弱ISC细胞谱系定向能力及相关基因表达,揭示心理压力通过引发ISC 内在缺陷和线粒体稳态失衡影响其分泌谱系分化(图1)。
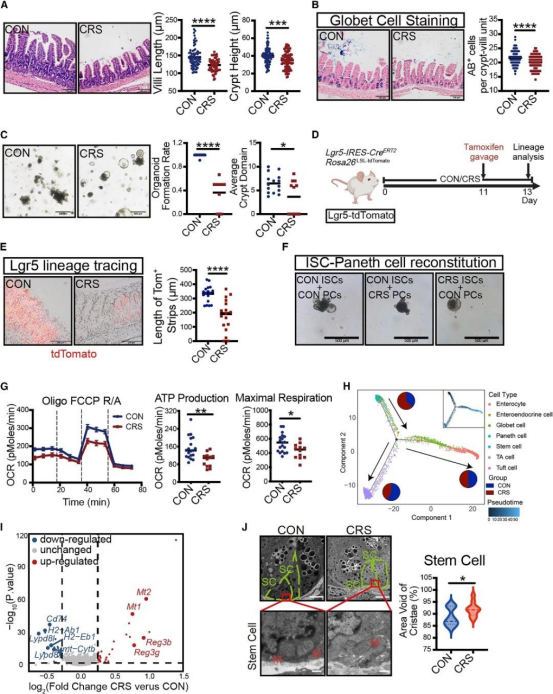
图1
2、压力借肠道微生物致肠道干细胞缺陷
为探究压力信号向肠道干细胞分泌性分化的传递机制,作者排除热量摄入干扰后发现,CRS小鼠回肠去甲肾上-腺素增加(血清皮质醇未变),α/β肾上-腺素受体阻滞剂可缓解其隐窝缩小和杯状细胞减少。综上,肠道菌群失衡是压力驱动ISC命运决策的重要因素(图2)。
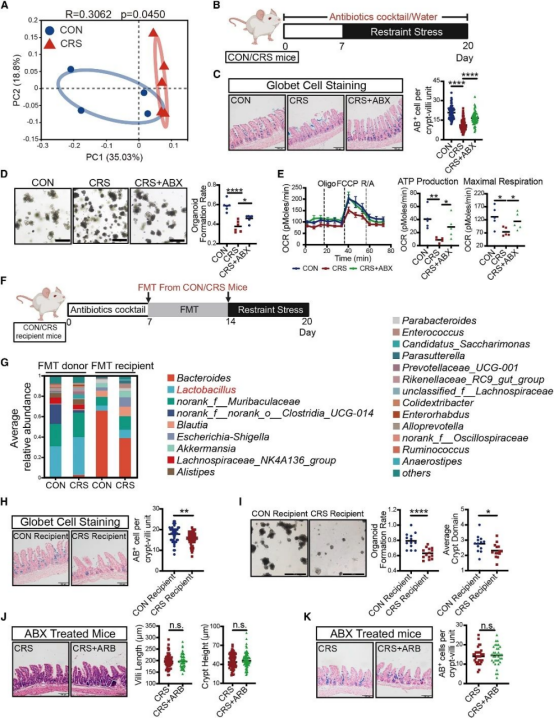
图2
3、特定乳酸杆菌菌株引发应激性肠道干细胞功能障碍
为筛选介导CRS效应的微生物,作者排除热量摄入干扰并重塑肠道菌群,发现氨苄青霉素、万古霉素和新霉素可削弱CRS对绒毛长度的影响,仅氨苄青霉素缓解隐窝损失,提示革兰氏阳性菌在应激性肠隐窝缺陷中起关键作用。在无菌小鼠中定殖特定乳酸杆菌菌株发现,L. murinus定殖小鼠应激后出现肠道结构损伤和分泌细胞减少,而 L. reuteri定殖小鼠具保护作用,表明乳酸杆菌属特定成员可驱动应激诱导的肠隐窝功能障碍(图 3)。
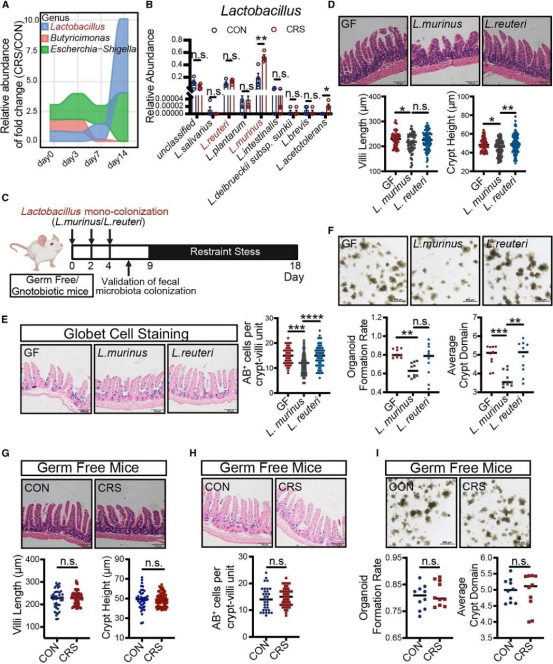
图3
4、细菌代谢物IAA传递应激信号阻碍肠道干细胞分化
为探究CRS对肠道代谢信号的影响,研究者对CRS小鼠回肠内容物进行代谢组学测序,发现吲哚乙酸(IAA)水平显著升高。进一步研究显示,L.murinus可将色氨酸转化为IAA,而 L.reuteri 不能。无菌小鼠定植L.murinus 后粪便IAA升高,且IAA处理可降低出芽率、减少潘氏细胞和肠内分泌细胞,并抑制线粒体功能。构建含IAA合成基因的大肠杆菌定植小鼠后,应激诱导的ISC缺陷加剧。综上,微生物代谢物IAA是应激条件下导致ISC功能障碍的关键介质(图 4)。
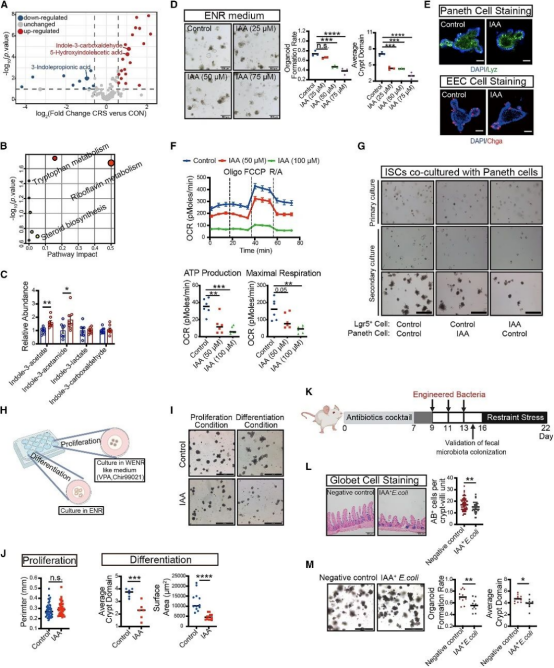
图4
5、IAA损害肠道干细胞线粒体生物能学功能
为探究IAA对ISC线粒体功能的分子作用机制,研究通过整体及单细胞RNA测序发现,IAA通过芳烃受体(AhR)通路上调外源物质代谢相关基因,降低肠道线粒体活性氧及呼吸链复合物 II 活性,下调线粒体完整性与代谢相关基因表达,引发线粒体形态改变。KEGG分析显示其显著影响氧化磷酸化(OXPHOS)功能。综上,IAA破坏线粒体稳态损害ISC功能,模拟应激对肠道的作用(图5)。
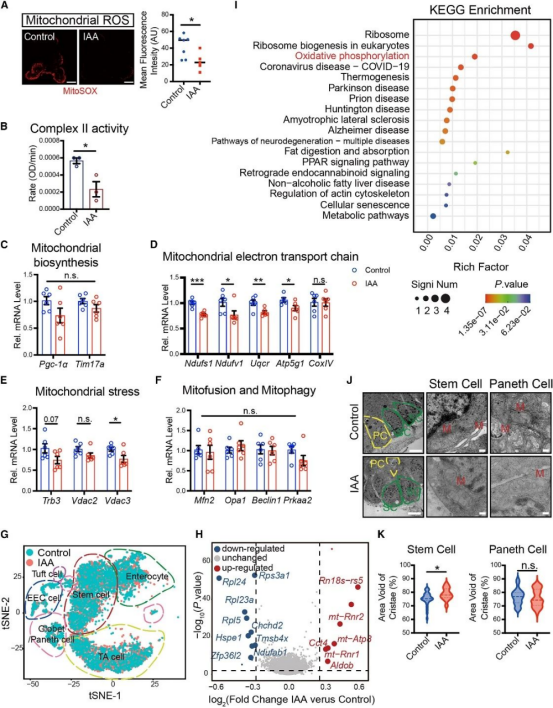
图5
6、IAA损害肠道干细胞线粒体生物能学功能
为探究IAA和应激对ISC分化代谢通路的重塑机制,研究者通过PCR和代谢组学发现,IAA处理可改变TCA循环和谷氨酸代谢,减少TCA中间产物。同位素追踪显示其抑制谷氨酸衍生的 TCA代谢物,对葡萄糖来源代谢物影响较小。通过丙酮酸脱氢酶激酶抑制剂DCA、补充谷氨酸或 α-KG干预发现,DCA和α-KG可逆转生长抑制,α-KG能缓解应激性肠道上皮损伤。综上,增强α-KG利用的代谢干预可有效改善 IAA和应激所致的ISC功能障碍(图 6)。
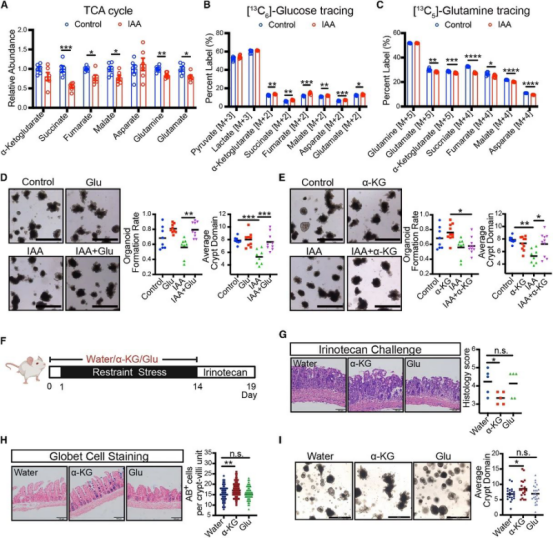
图6
7、心理应激患者体内普遍存在吲哚乙酸(IAA)
为验证研究的临床相关性,研究者分析健康对照组(HC)和重度抑郁症(MDD)患者的肠道微生物数据发现,MDD患者粪便中乳酸菌属丰度及吲哚乙酸(IAA)水平显著升高,IAA前体IAM 浓度降低,且 MDD合并便秘患者IAA水平更高。进一步纳入双相躁狂症(BM)、双相抑郁症(BD)患者分析显示,BM患者乳酸菌丰度显著增加,MDD和BD患者肠道微生物中IAA生物合成基因显著富集。综上,心理应激患者肠道内IAA生成能力普遍增强,可能与肠道合并症发生相关(图7)。
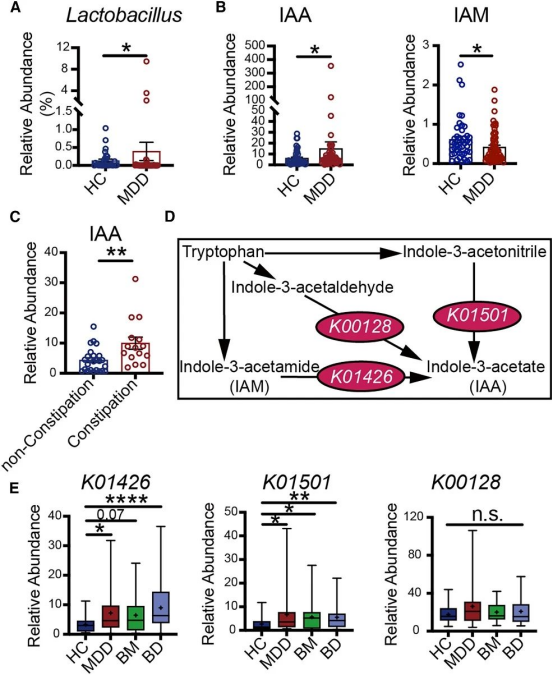
图7
研究总结
心理压力对脑肠轴影响机制尚不明确。该团队利用微生物宏基因组学、单细胞测序、代谢组学等多组学技术发现,乳酸杆菌代谢产物IAA可通过阻碍线粒体呼吸,干扰肠道干细胞(ISC)命运抉择及肠道上皮更新,靶向IAA或可成为干预应激相关脑肠综合征的潜在策略。